12月30日,由中國(guó)海洋大學(xué)、逢時(shí)(青島)海洋科技股份有限公司共建的海洋磷脂醫(yī)藥創(chuàng)新聯(lián)合研究中心正式揭牌。中國(guó)海洋大學(xué)校長(zhǎng)張峻峰,逢時(shí)科技創(chuàng)始人、董事長(zhǎng)高以成出席活動(dòng)并致辭,高校科研團(tuán)隊(duì)代表及企業(yè)技術(shù)骨干共同見證這一時(shí)刻。

中國(guó)海洋大學(xué)-逢時(shí)科技海洋磷脂醫(yī)藥創(chuàng)新聯(lián)合研究中心成立
名校名企強(qiáng)強(qiáng)聯(lián)合,筑牢產(chǎn)業(yè)創(chuàng)新根基
中國(guó)海洋大學(xué)作為國(guó)家“雙一流”A類建設(shè)高校,在海洋和水產(chǎn)學(xué)科領(lǐng)域具有顯著優(yōu)勢(shì)。作為我國(guó)海洋生物醫(yī)藥領(lǐng)域的“領(lǐng)頭羊”,中國(guó)海洋大學(xué)醫(yī)藥學(xué)院擁有國(guó)家海洋藥物工程技術(shù)研究中心、海洋藥物教育部重點(diǎn)實(shí)驗(yàn)室等頂尖平臺(tái),牽頭成立青島海洋生物醫(yī)藥研究院,構(gòu)建了從藥物發(fā)現(xiàn)、評(píng)價(jià)、研發(fā)到產(chǎn)業(yè)化的完整體系,是國(guó)家“藍(lán)色藥庫(kù)”開發(fā)的核心力量。
目前,全球已上市的16個(gè)海洋創(chuàng)新藥物中,中國(guó)占據(jù)的2席——抗心腦血管疾病藥物藻酸雙酯鈉、治療阿爾茨海默病的甘露特鈉膠囊,均源自中國(guó)海大;該校研發(fā)的抗腫瘤新藥BG136也已進(jìn)入臨床階段。該校在多糖寡糖、肽類等海洋活性物質(zhì)提取與修飾上具備行業(yè)優(yōu)勢(shì),并將脂質(zhì)開發(fā)作為未來最重要的研究方向之一,還布局了合成生物學(xué)等前沿方向,擁有藥化、藥理、藥分、藥劑等全方位完整研發(fā)體系,可為海洋藥物創(chuàng)新提供堅(jiān)實(shí)支撐。
作為國(guó)家級(jí)專精特新“小巨人”企業(yè),逢時(shí)科技在海洋生物醫(yī)藥產(chǎn)業(yè)落地承接方面表現(xiàn)突出。自去年12月26日逢時(shí)海洋醫(yī)藥研創(chuàng)產(chǎn)業(yè)基地落成投用以來,企業(yè)研發(fā)團(tuán)隊(duì)聚焦海洋磷脂高值化利用與醫(yī)藥轉(zhuǎn)化,持續(xù)推進(jìn)工藝開發(fā)與迭代優(yōu)化。

逢時(shí)海洋醫(yī)藥研創(chuàng)產(chǎn)業(yè)基地
逢時(shí)科技海洋醫(yī)藥研發(fā)總監(jiān)鄧學(xué)鵬介紹,逢時(shí)科技獨(dú)有的凍蝦提油技術(shù),使EPA含量提升40%;在此基礎(chǔ)上進(jìn)一步提純,可得到符合藥用輔料甚至原料藥標(biāo)準(zhǔn)的高純磷蝦磷脂。這為磷蝦磷脂藥用輔料、南極磷蝦多烯磷脂酰膽堿原料藥的規(guī)模化生產(chǎn)筑牢了技術(shù)根基。其中,藥用輔料可作為藥物遞送載體開發(fā)脂質(zhì)體、磷脂復(fù)合物、脂質(zhì)納米顆粒(LNP)等高端制劑,原料藥則可用于開發(fā)降血脂、治療肝損傷及阿爾茨海默病等疾病的藥物,展現(xiàn)出強(qiáng)勁的產(chǎn)業(yè)轉(zhuǎn)化能力。
助力最為前沿的核酸藥物開發(fā),產(chǎn)學(xué)研協(xié)同攻堅(jiān)高端制劑
此次揭牌的海洋磷脂醫(yī)藥創(chuàng)新聯(lián)合研究中心,將精準(zhǔn)聚焦海洋磷脂作為原料藥和藥用輔料的應(yīng)用難題,重點(diǎn)圍繞磷蝦磷脂的乳化行為及制劑穩(wěn)定性研究、磷蝦磷脂的生物學(xué)功能與安全性評(píng)價(jià)以及磷蝦磷脂用于核酸藥物遞送等方向開展系統(tǒng)性攻關(guān),致力于打通從基礎(chǔ)海洋資源到高端制劑的全鏈條技術(shù)路徑,助力我國(guó)突破LNP(脂質(zhì)納米顆粒)、納米脂肪乳等高端制劑核心脂質(zhì)材料長(zhǎng)期依賴進(jìn)口的“卡脖子”困境。
此次合作將助力青島在最為前沿的核酸藥物開發(fā)這片產(chǎn)業(yè)藍(lán)海中率先布局。作為繼小分子化藥、蛋白類生物藥(單抗、融合蛋白、ADC等)的第三代藥物類型,核酸藥物通過調(diào)控基因表達(dá)精準(zhǔn)治療疾病,且具有長(zhǎng)效性、研發(fā)周期短等特點(diǎn),已成為生物醫(yī)藥領(lǐng)域的顛覆性前沿方向。數(shù)據(jù)顯示,預(yù)計(jì)2030年,全球核酸藥物市場(chǎng)規(guī)模將超500億美元。
作為核酸藥物的關(guān)鍵遞送載體,LNP(脂質(zhì)納米顆粒)是一種由多種脂質(zhì)自組裝形成的“微小包裹體”,能為核酸藥物提供“保護(hù)膜”,使其不被體內(nèi)降解并高效進(jìn)入細(xì)胞,具有生物相容性好、免疫原性低、遞送效率高等顯著優(yōu)勢(shì)。在LNP的構(gòu)成中,磷脂承擔(dān)了“搭骨架”和“仿生膜”作用,可維持顆粒結(jié)構(gòu)穩(wěn)定、提升細(xì)胞攝取效率。然而,現(xiàn)在制備LNP所用傳統(tǒng)陸源磷脂(大豆磷脂和蛋黃卵磷脂)具有炎癥和過敏反應(yīng)風(fēng)險(xiǎn)。
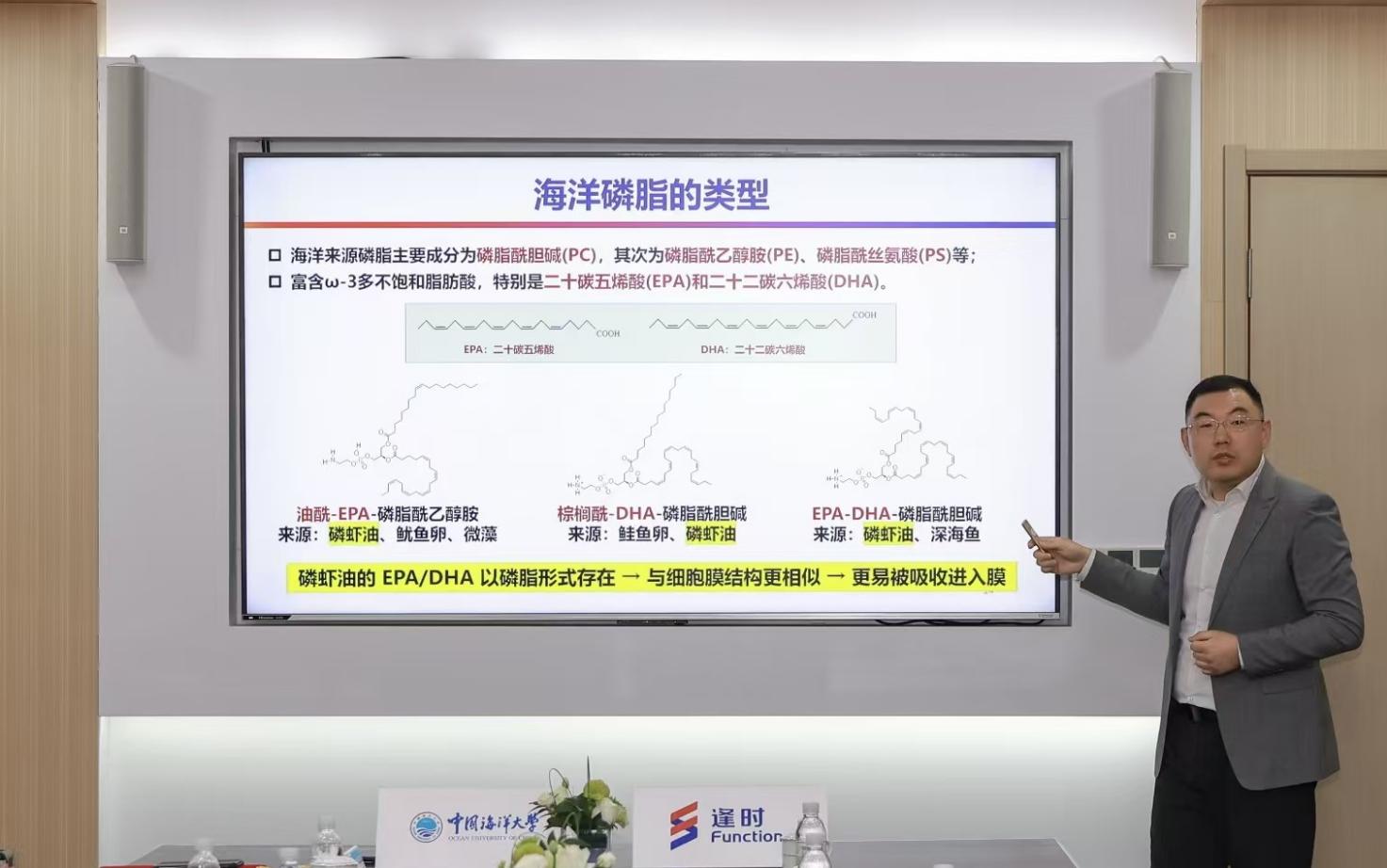
中國(guó)海洋大學(xué)醫(yī)藥學(xué)院教授姜帥介紹海洋磷脂醫(yī)藥創(chuàng)新聯(lián)合研究中心研究?jī)?nèi)容
而此次合作錨定的南極磷蝦提取海洋磷脂,可為新型LNP研發(fā)提供優(yōu)質(zhì)磷脂原料支撐。其DHA、EPA以磷脂結(jié)合型存在,更接近人體細(xì)胞膜結(jié)構(gòu),不僅能提升LNP遞送效率,還具備抗炎、抗氧化特性。
未來,中國(guó)海洋大學(xué)將側(cè)重分子機(jī)理、結(jié)構(gòu)改造和遞送規(guī)律研究,逢時(shí)科技則負(fù)責(zé)規(guī)模化制備和產(chǎn)業(yè)轉(zhuǎn)化,通過產(chǎn)學(xué)研協(xié)同推進(jìn)LNP在mRNA、siRNA等核酸藥物中的應(yīng)用驗(yàn)證與制劑優(yōu)化,為核酸藥物產(chǎn)業(yè)發(fā)展注入新動(dòng)能。
以校企合作搭建起創(chuàng)新與產(chǎn)業(yè)深度融合的橋梁,逢時(shí)科技與中國(guó)海大將協(xié)同推進(jìn)高純度藥用級(jí)海洋磷脂的工藝開發(fā)、納米脂肪乳和靶向遞送系統(tǒng)應(yīng)用,共同致力于將海洋磷脂打造成為“藍(lán)色藥庫(kù)”的又一標(biāo)志性成果。這一舉措不僅將加速海洋生物醫(yī)藥科技成果落地轉(zhuǎn)化,更將為落實(shí)國(guó)家“藍(lán)色藥庫(kù)”戰(zhàn)略、發(fā)展新質(zhì)生產(chǎn)力、建設(shè)“海洋強(qiáng)國(guó)”提供堅(jiān)實(shí)的科技與產(chǎn)業(yè)支撐,助力青島在海洋生物醫(yī)藥領(lǐng)域持續(xù)領(lǐng)跑,書寫海洋經(jīng)濟(jì)高質(zhì)量發(fā)展的新篇章。



